Nedostatek železa (Fe)
Definice: je anémie z nedostatku železa (Fe), patří mezi nejčastější hematologické onemocnění. Jde o důsledek nedostatku hemoglobinu, což vede k narušení zásobování tkání kyslíkem.
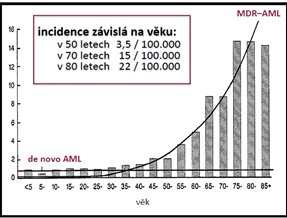
Epidemiologie: Prevalence v ČR: 8 – 20 % u žen a 5 % u mužů
Etiopatogeneze:
Etiologie:
- Zvýšená potřeba železa s nedostatečnou kompenzací:
- Novorozenci a adolescence
- Těhotenství (900 – 1000 mg Fe) a laktace (1mg denně)
- U nemocných dostávajících erytropoetiny (= funkční sideropenie)
- Akcelerovaná erytropoesa
- Zvýšené ztráty železa:
- Fyziologicky:
- menstruace (40 – 60ml = 16 – 25mg železa) kompenzace je, že se zvýší denní resorpce železa z potravy ze 7 – 10% na 20 – 25% přijaté dávky železa, ale při krevních ztrátach 70 – 80ml krve již nestačí kompenzovat zvýšenou resorpcí
- porod
- Patologicky: chirurgické výkony, GIT ztráty, hematurie, hemoptýza
- Iatrogeně: časté odběry, léky (kys. acetylsalicylová, glukokortikoidy, nesteroidní antirevmatika)
- Dárci (ztráta cca 150 – 200mg Fe)
- Fyziologicky:
- Snížený příjem či porucha absorpce:
- Vegetariani nebo obecně malnutrice
- Malabsorpční syndromy: celiakie, Crohnova choroba
- Po chirurgickém výkonu na žaludku či střevech – resekce
- Střevní parasitosa (ankylostomiasa)
- Helicobacter pylori
- Autoimmunní atrofická gastritida (nízká HCL)
Vstřebávání železa (Fe):
- Absorbuje se dvojmocné železo (Fe2+,) lépe jako hem z masa a orgánů
- Absorpce je zvýšená v těhotenství a zvýšené erytropoese
- Absorpce je snížená u stavů s přetížením Fe, zánětů
- Absorpci zvyšují: vitamin C, některé cukry
- Absorpci snižují: phytaty (v zelenině), čaje
Patogeneze:
Při rozvoji sideropenie rozeznáváme tři stadia:
- Prelatentní sideropenie (nedostatečné zásoby Fe): postupné vyčerpaní zásob železa, ale dodávka pro potřeby erytropoézy je ještě dostatečná
- snížená koncentrace feritinu v séru
- sérové železo v normě
- hemoglobin v normě
- Latentní sideropenie (erytropoéza uskutečňována při nedostatku Fe): zásoby železa jsou zcela vyčerpány a je snížena jeho dodávka do erytroblastů kostní dřeně, prozatím nelimituje proliferaci buněk
- snížená koncentrace feritinu v séru
- snížené sérové železo
- hemoglobin v normě
- Manifestní sideropenie (anemie z nedostatku Fe): nedostatek Fe tlumí proliferaci a vzniká anémie
- snížená koncentrace feritinu v séru
- snížené sérové železo
- snízený hemoglobin
Klinický obraz:
- únava a snížená výkonnost
- tachykardie
- kožní projevy: atrofie kůze
- snížené intelektuální schopnosti
- dysfagie
- deprese
- časté infekce
- bledost kůže a sliznic
- koilonychie – lžičkovité nehty jsou tenké a mají vyvýšené okraje
- zvýšená lomivost nehtů
- angulární cheilosa – zánět rtu
- rudý, vyhlazený (atrofický) jazyk
- glositida
- padání vlasů (alopecia areata)
Diagnóza:
- Anamnéza a fyzikální vyšetření
- Laboratorní vyšetření:
- laboratorní testy:
- nejdůležitěší je hladina sérového ferritinu (zásobní protein železa) a solubilního transferinového receptoru (saturace transferinu): obě vyšetření jsou zasadní pro diagnózu: odhalí 95% pacientů s latentní sideropenii
- sérové železo
- transferrin
- vazebná kapacita
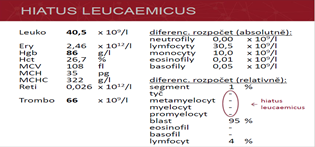
- krevní nátěr: hypochromie, mikrocytóza
- Mikrocytární: protože zrání erytroblastů je prodloužene → projdou větším počtem mitotických dělení → zmenšení jejich objemu/průměru
- hypochromní: protože ak je nedostatek Fe hodně tak nejsou ani dostatečně hemogloginizovány
- Diferenciální diagnóza mikrocytózy:
- sideropenie
- thalassemie
- Haemoglobinopathie (E,C,CS, Lepore…)
- Anemie chronických nemocí
- Familiární sideroblastická anemie
- Různé (otrava olovem)
- laboratorní testy:
- Ďalší vyšetření závisí na anamnéze a symptomatologii:
- Okultní krvácení
- Gastrointestinální vyšetření – endoskopie
- Gynekologické vyšetření
Nález u latentní sideropenie:
- Hladina feritinu je snížena pod 12µg/l
- Snížena hladina Fe
- Zvýšená celková vazebná kapacita transferinu pro Fe
- Saturace transferinu klesá pod 16%
- Zvýšená koncentrace solubilních transferinových receptorů v séru
- Zvýšená koncentrace volného protoporfyrinů v śeru
- V kostní dřeni klesá počet sideroblastů pod 30%
Nález u manifestní sideropenie:
- Hypochromní mikrocytární sideropenie
- Hladina feritinu je snížena pod 5µg/l
- Saturace trasnferinu klesá pod 10%
- V kostní dřeni mené než 10% sideroblastů
Diferenciální diagnostika nedostatku železa:

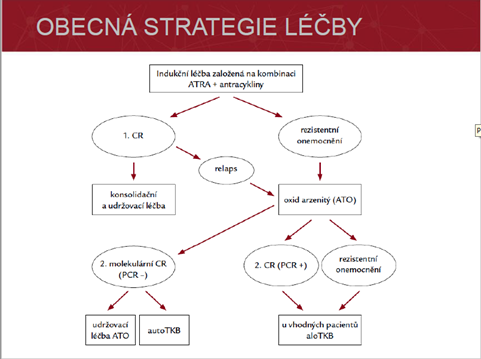
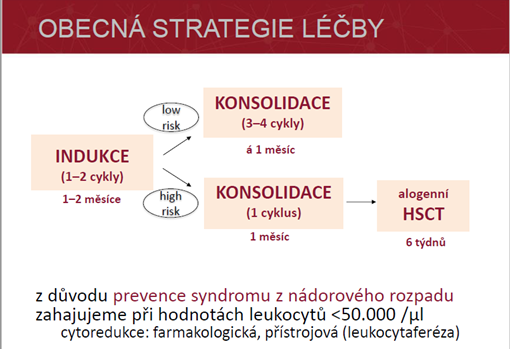
Terapie:
- Ostranění příčiny a substituce Fe
- Substituce železa:
- Preparáty Fe (100 – 200mg/den) → z toho se vstřebe 50 – 60mg a dojde k vzestupu hemoglobinu o 2g/l denně
- Železo podávame rovnoměrně během dne – nalačno ½ hodinu před jídlem, nebo 2 hodiny po jídle
- Délka podávání se vztahuje k trvání příčiny a hloubce sideropenie
- V případě intolerance či poruše absorpce se aplikuje Fe parenterálně
Pro zajímavost:
Základní údaje k metabolismu Fe: 3500 – 5000mg
- Celkové množství Fe v těle – 3,5 – 5 g:
- erytrocyty_hemoglobin: 2500 mg
- erytroblasty: 150mg
- enzymy: 150mg
- myoglobin: 300mg
- hepatocyty: 250mg
- makrofagy: 500 mg
- Denní absorpce: 1 – 2 mg / denní ztráty: 1 – 2 mg (delicate balance)
- Denní průměrné množství v jídle: 10 – 15g (absorbed only Fe2+ 10%)
- Fe není rozpustný, vždy je vázáno na proteiny: ferroportin, transferin, ferritin
- Ferroportin je transmembránový protein, který čerpá železo z buněk. Nachází se na povrchu buněk, kde transportuje nebo skladuje železo
- Samotné Fe je velmi toxické
- Hepcidin – je regulátor metabolismu Fe, syntéza v játrech