Preleukemie
Dřeňový útlum
Definice: je klonální porucha krvetvorby. V časné fázi obraz buněčně bohaté kostní dřeně se současnou cytopenií v periferní krvi. V pozdní fázi obraz bohaté kostní dřeně s nárůstem počtu myeloblastů – leukemizace procesu.
Epidemiologie: 4,5/100.000, výskyt stoupa s věkem – ↑ nad 60let
Dělení: WHO klasifikace:
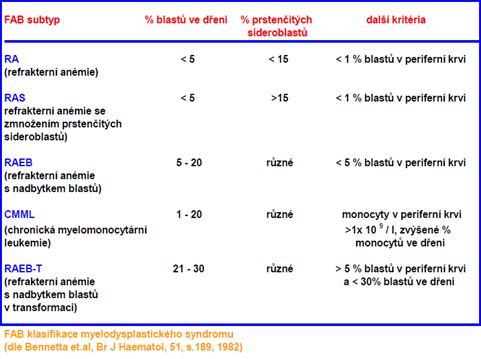
- Myelodysplastický syndrom
- Refrakterní anémie (RA)
- Refrakterní anémie s prstenčitými sideroblasty (RARS)
- Refrakterní cytopenie s dysplasií ve více řadách (RCMD)
- Refrakterní anémie se zmnožením blastů (RAEB):
- RAEB I. ( < 10% blastů)
- RAEB II. ( > 10% blastů)
- 5q – syndrom (izolovaná delece 5q)
- Myelodysplastický syndrom neklasifikovaný
Etiopatogeneze:
Patogeneze:
NOXA (virus, toxin, onkoprotein) → poškození kmeňové krvetvorné buňky → vznik mutace → možnost vzniku patologického klonu buněk z poškozené kmeňové krvetvorné buňky → RŮSTOVÁ VÝHODA KLONU → možnost postupného nahrazení normální krvetvorby patologickým klonem
OBRANNÁ REAKCE ORGANISMU: za normálních okolností vede k eliminaci poškozené buňky. Abnormální obranná reakce – může vést k nadprodukci cytokinů uplatňujících se v procesu buněčné smrti – apoptosy a v abnormální reakci T lymfocytů, jež může podporovat růst patologického klonu.
MUTACE:
- ONKOGENY :
- Za normálních okolností nejsou exprimovány v genomu, jejich abnormální exprese v důsledku mutace může vést k aktivaci abnormální metabolické cesty, jež ve svém důsledku může mít pro buňku růstovou výhodu (např. abnormální aktivace tyrosin kinasy → kontinuální stimulace proliferace).
- ANTIONKOGENY /tumor supresorické geny/:
- Jsou za normálních okolností exprimovány v genomu a uplatňují se ve fyziologických pochodech (např. proces buněčné smrti – apoptosy).
- Ztráta jejich exprese v důsledku mutace může vést k abnormální proliferaci nezávislé na regulačních faktorech.
- ČASNÁ FÁZE MDS:
- Mutace vedoucí ke vzniku patologického klonu vede k poruše reparačních mechanismů buňky a k abnormální imunitní odpovědi → stimulace proliferace časných prekursorů a zvýšená apoptóza zralejších elementů krvetvorby (účinkem některých cytokinů).
- Obraz buněčně bohaté kostní dřeně se současnou cytopenií v periferní krvi.
- POZDNÍ FÁZE MDS:
- Nestabilita genomu (změny karyotypu) vedoucí k přibývání mutací.
- Zvýšená incidence mutací onkogenů, podporujících abnormální proliferaci a inhibujících fyziologickou diferenciaci časných prekursorů → progresivní nárůst počtu nezralých CD 34+ prekursorů v kostní dřeni náležících k patologickému klonu.
- Obraz bohaté kostní dřeně s nárůstem počtu myeloblastů – leukemizace procesu.
Klinický obraz: od anemických symptomů přes infekční komplikace až k různě těžkým krvácivým projevům
Diagnóza:
- Periferní krevní obraz : cytopenie (různě vyjádřená v krevních řadách)
- Sternální punkce : aspirace
- morfologie – dysplastické změny – atypie jádra, nesouběh zrání jádra a cytoplasmy, poruchy granulací a barvitelnosti cytoplasmy, megaloidie), buněčnost, procento blastů
- cytochemie – barvení na Fe → prstenčité sideroblasty
- cytogenetika – počet a charakter abnormit karyotypu – nejčastěji abnormity 5,7,8 chromosomu, mnohotné aberace
- průtoková cytometrie – počet CD34+ prekursorů (nezralé myeloidní prekurzory)
- kultivace dřeně in vitro, molekulární biologie
- Trepanobiopsie dřeně : buněčnost, topické změny, fibrosa
- Biochemická vyšetření: Fe, feritin, B12, erytropoetin, bilirubin, koagulace, vyšetření CD 55- a CD59- erytrocytů, testy na korpuskulární a extrakorpuskulární hemolysu
- Celkové vyšetření nemocného – k vyloučení sekundárních hematologických změn při onemocnění jiného orgánu
Diferenciální diagnóza:
1. APLASTICKÁ ANÉMIE: hypocelulární dřeň bez dysplastických změn, nejsou přítomny změny karyotypu a cytochemické změny, nejsou přítomny CD 59 erytrocyty, nejsou zmnoženy blasty, není přítomna fibrosa dřeně.
2. PAROXYSMÁLNÍ NOČNÍ HEMOGLOBINURIE: je přítomna intravaskulární hemolysa s hemoglobinurií, jsou přítomny CD 59 a CD 55 erytrocyty, nejsou přítomny změny karyotypu.
3. AKUTNÍ LEUKÉMIE: je přítomno více než 30% blastů (více než 20% blastů dle nové WHO klasifikace), nejsou dysplastické změny (pokud nejde o leukémii přechodem z MDS).
4. MEGALOBLASTOVÉ ANÉMIE: je nápadná megaloblastová přestavba dřeně bez ďalších dysplastických změn, nejsou přítomny změny karyotypu a cytochemické změny, je přítomen deficit B12, kys. listové, celkové příznaky (glositis, neurologické příznaky), nález v GIT (atrofická gastritis, malabsorpce)
5. SIDEROBLASTICKÉ ANÉMIE: vrozené a získané formy (otrava olovem, některé infekce a léky). Nejsou změny karyotypu, charakteristická anamnesa.
Terapie:
Medzinárodní prognostický systém (IPPS): rozdelí pacientov do 4 skupin podle rizik přechodu do AML podle počtu blastů v dřeni, cytopenii a karyotypu:
- Nízke riziko → konzervativni terapie
- Intermediární – 1 → konzervativni terapie
- Intermediární – 2 → chemoterapie, alotransplantace
- Vysoké → chemoterapie, transplantace
Konzervativni terapie:
- Podpůrná terapie:
- transfúze erytrocytů, trombocytů, vitaminů B
- chelatační terapie při přetížení železem
- Látky inhibující stupeň apoptózy:
- kortikosteroidy
- růstové faktory (EPO, G – CSF = granulocyty stimulujíci faktor)
- Imunosupresivní látky: kortikosteroidy + Cyklosporin A
- prednison 20 – 30mg/den + CS-A 3 mg/kg/den
- antithymocytární globulin (ATG)
- lenalidomid (imunomodulační lék): při 5q-syndromů
- Hypometylační látky: 5 – azacytidin, decitabin – reverse vyhasínání funkce diferenciačních genů (p15) → snížení počtu blastů, prodloužení doby do leukemizace procesu
- Chemoterapie:
- monoterapie: hydroxyurea, cytosin arabinosid
- nízké dávky: 10 – 40 mg/m2
- kombinovaná chemoterapie – anthracykliny + cytosin arabinosid
- standardní dávky: 100 – 200 mg/m2
- vysoké dávky 2 – 3 g/m2
- monoterapie: hydroxyurea, cytosin arabinosid
- Transplantace krvetvorných buněk: allogení od HLA identického příbuzného či nepříbuzného dárce, v současné době jediný kurativní přístup
- poměrně vysoké riziko komplikací při transplantaci (25 – 40%) – infekce, reakce štěpu proti hostiteli
Mladši nemocní s pokročilým MDS → kombinovaná chemoterapie (jako u AML) a následně alogenní transplatace